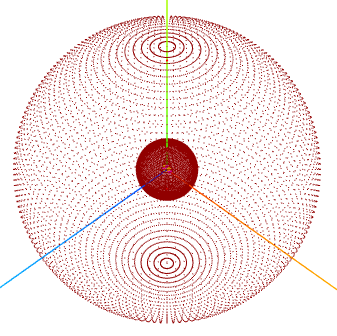
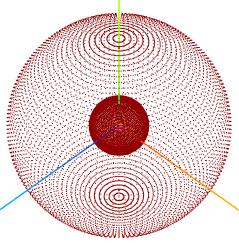
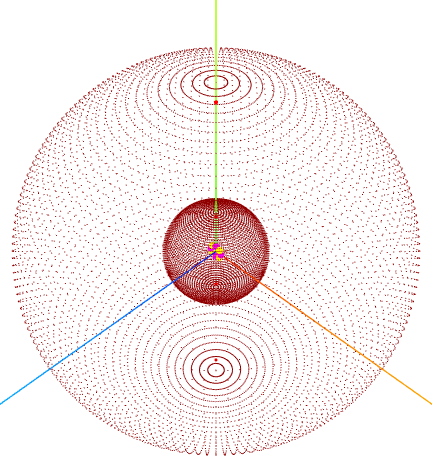
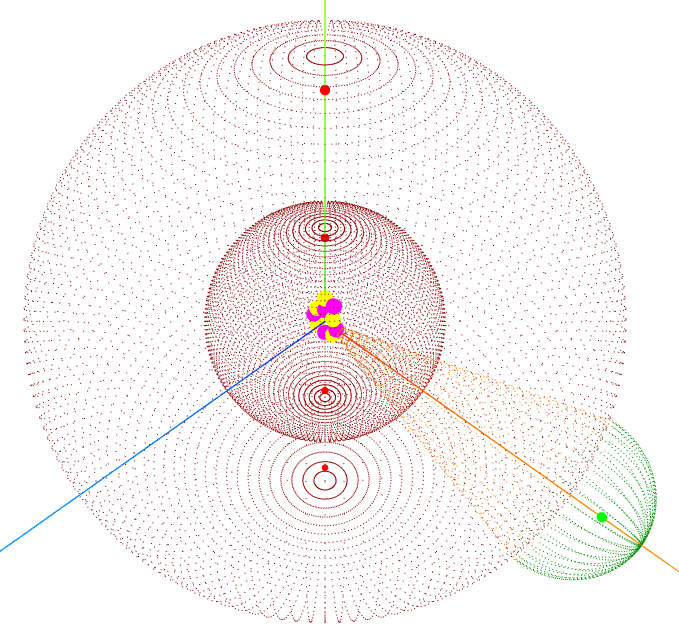
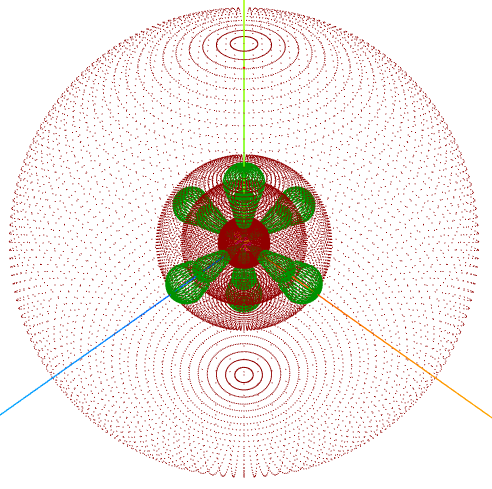
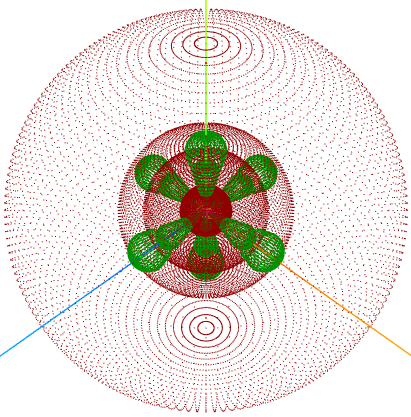
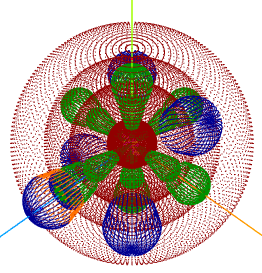
Este curso foi produzido com nosso aplicativo " OA3D - Orbitais Atômicos 3D" responsável pelas imagens aqui apresentadas.
OA3D pode ser executado aqui.
São 7 capítulos correspondentes do primeiro ao sétimo período da tabela periódica, contendo imagens e textos dos elementos, visando o entendimento de sua estrutura de orbitais atômicos.
É utilizada uma escala com o deslocamento focal da câmera, com a característica de ser inversamente proporcional ao tamanho da imagem. Quando menor o valor da escala, correspondente ao deslocamento focal da câmera, maior ficará a imagem, pois mais próxima estará a câmera do átomo focado.
Esta escala é chamada Escala DFC, ou Escala de Deslocamento Focal da Câmera, ou simplemente DFC, e a unidade de medida da escala é nanometro (nm).
Por exemplo com o hidrogênio com Escalas DFC de 800 nm e 200 nm.
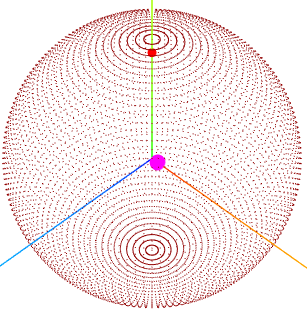
Escala DFC: 200 nm. Hidrogênio.
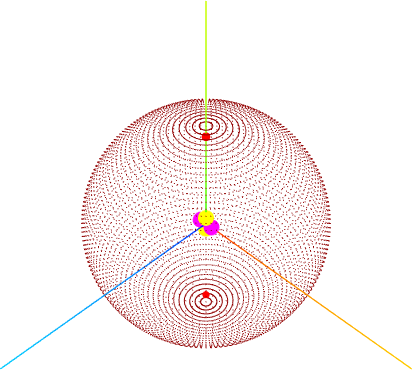
Escala DFC: 800 nm. Hidrogênio.
O valor padrão de escala utilizado é de 800 nm, para permitir a captura de tela da imagem do átomo do Frâncio, de Z = 87 e maior raio atômico da tabela periódica.
Escala DFC: 800 nm. Frâncio.
O primeiro período na tabela periódica contém os elementos hidrogênio e hélio.
Orbital 1s
Hidrogênio (H)
Z: 1 (1 e-1 1 p+1 0 n0)
Configuração eletrônica: 1s1
DFC: 200 nm. Hidrogênio. Observe nessa escala o elétron (em vermelho) e o próton (em roxo) do H.
DFC: 800 nm.
Hélio (He)
Z: 2 (2 e-1 2 p+1 2 n0)
Configuração eletrônica: 1s2
Os dois elétrons no orbital s do hélio completam a camada de valência do primeiro período, único com a valência completa com o orbital s.
DFC: 200 nm. Hélio. Com a câmera mais próxima do He vemos os 2 elétrons (vermelho), no núcleo 2 prótons (roxo) e 2 nêutrons (amarelo).
DFC: 800 nm. Hélio.
O terceiro período da tabela periódica contém os elementos com Z de 11 a 18, respectivamente sódio, magnésio, alumínio, silício, fósforo, enxofre, cloro e argônio.
A configuração eletrônica [He] 2s2 2p6 do neon, último elemento do segundo período, será representada por [Ne].
Orbital 3s
Sódio (Na)
Z: 11 (11 e-1 11 p+1 11 n0)
Configuração eletrônica: [Ne] 3s1
DFC: 800 nm. Sódio.
DFC: 800 nm. hidrogênio.
Abaixo podemos comparar os raios atômicos do sódio, do Lítio e do hidrogênio, respectivamente, com a câmera bem distante, demonstrando que o raio atômico é uma propriedade periódica que aumenta de cima para baixo na tabela periódica.
DFC: 3000 nm. Sódio, lítio e hidrogênio.
Magnésio (Mn)
Z: 12 (12 e-1 12 p+1 12 n0)
Configuração eletrônica: [Ne] 3s2
DFC: 800 nm. Magnésio.
Orbital 3p
Alumínio (Al)
Z: 13 (13 e-1 13 p+1 13 n0)
Configuração eletrônica: [Ne] 3s2 3p1
DFC: 800 nm. Alumínio. Primeiro orbital 3p (3p1).
Silício (Si)
Z: 14 (14 e-1 14 p+1 14 n0)
Configuração eletrônica: [Ne] 3s2 3p2
DFC: 800 nm. Silício. Segundo orbital 3p (3p2).
Fósforo (P)
Z: 15 (15 e-1 15 p+1 15 n0)
Configuração eletrônica: [Ne] 3s2 3p3
DFC: 800 nm. Fósforo. Terceiro orbital 3p (3p3).
Enxofre (S)
Z: 16 (16 e-1 16 p+1 16 n0)
Configuração eletrônica: [Ne] 3s2 3p4
DFC: 800 nm. Silício. Quarto orbital 3p (3p4).
Cloro (Cl)
Z: 17 (17 e-1 17 p+1 17 n0)
Configuração eletrônica: [Ne] 3s2 3p5
DFC: 800 nm. Cloro. Quinto orbital 3p (3p5).
Argônio (Al)
Z: 18 (18 e-1 18 p+1 18 n0)
Configuração eletrônica: [Ne] 3s2 3p6
DFC: 800 nm. Argônio. Sexto orbital 3p (3p6).
O segundo período da tabela periódica tem os elementos com Z de 3 a 10.
São respectivamente os elementos lítio, berílio, boro, carbono, nitrogênio, oxigênio, flúor e neon.
A configuração eletrônica 1s2 do hélio, último elemento do primeiro período, será representada por [He].
Orbital 2s
Lítio (Li)
Z: 3 (3 e-1 3 p+1 3 n0)
Configuração eletrônica: [He] 2s1
DFC: 800 nm. Lítio.
O raio atômico é uma propriedade periódica dos átomos que cresce no sentido de cima para baixo, nos grupos da tabela periódica, junto com o crescimento dos períodos.
O raio atômico do lítio é muito maior do que o do hidrogênio, mostrado abaixo, na mesma escala do lítio, permitindo a visualização do raio atômico bem maior do lítio em relação ao do hidrogênio.
DFC: 800 nm. Hidrogênio. Para comparação com o lítio.
DFC: 800 nm. Hélio. Agora orbital 1s do lítio, camada de valência completa.
DFC: 450 nm. Lítio. Com a proximação de câmera de 800 para 450 nm podemos ver os 3 elétrons (vermelhos), 3 prótons (roxos) e nêutrons (amarelos).
Berílio (Be)
Z: 4 (4 e-1 4 p+1 4 n0)
Configuração eletrônica: [He] 2s2
Escala DFC: 800 nm. Berílio.
DFC: 450nm. Berílio.
Orbitais 2p
Boro (B)
Z: 5 (5 e-1 5 p+1 5 n0)
Configuração eletrônica: [He] 2s2 2p1
DFC: 800 nm. Boro. 2 orbitais s e 1 orbital p.
DFC: 200 nm. Nesta escala podemos observar os 6 elétrons (4 vermelhos e 1 verde) , 5 prótons (roxos) e 6 nêutrons (amarelos).
Carbono (C)
Z: 6 (6 e-1 6 p+1 6 n0)
Configuração eletrônica: [He] 2s2 2p2.
DFC: 800 nm. Carbono. 2 orbitais s e 2 orbitais p.
Nitrogênio (N)
Z: 7 (7 e-1 7 p+1 7 n0)
Configuração eletrônica: [He] 2s2 2p3
DFC: 800nm. Nitrogênio. 2 orbitais s e 3 orbitais p.
Oxigênio (O)
Z: 8 (8 e-1 8 p+1 8 n0)
Configuração eletrônica: [He] 2s2 2p4
DFC: 800nm. 2 orbitais s e 4 orbitais p.
Flúor (F)
Z: 9 (9 e-1 9 p+1 9 n0)
Configuração eletrônica: [He] 2s2 2p5
DFC: 800 nm. Flúor. 2 orbitais s e 5 orbitais p.
Neon (Ne)
Z: 10 (10 e-1 10 p+1 10 n0)
Configuração eletrônica: [He] 2s2 2p6
DFC: 800 nm. Neon. 2 orbitais s e 6 orbitais p. Camada de valência completa. Gás nobre.
DFC: 100 nm. Núcleo do neon.
DFC: 200 nm. Neon. 10 élétrons (4 vermelhos e 6 verdes), 10 prótons (roxos) e 10 nêutrons (amarelos)
No quarto período da tabela periódica estão os elemento com Z de 19 a 36, respectivamente potássio e cálcio (4s); escândio, titânio, vanádio, crômio, manganês, ferro, cobalto, níquel, cobre e zinco (3d); gálio, germânio, arsênio, selênio, bromo e criptônio (4p).
A configuração eletrônica 1s2 2s2 2p6 3s2 3p6 do argônio será representada por [Ar].
Orbitais 4s
Potássio (P)
Z: 19 (19 e-1 19 p+1 19 n0)
Configuração eletrônica: [Ar] 4s1
DFC: 800 nm. Potássio. Primeiro elétron do orbital 4s.
Cálcio (Ca)
Z: 20 (20 e-1 20 p+1 20 n0)
Configuração eletrônica: [Ar] 4s2
DFC: 800 nm. Segundo elétron do orbital 4s.
Orbitais 3d
Os orbitais d são bilobulares (dois lóbulos) ou mono lobulares com um tórus.
Escândio (Sc)
Z: 21 (21 e-1 21 p+1 21 n0)
Configuração eletrônica: [Ar] 4s2 3d1
DFC: 800 nm. Escândio. Primeiro orbital 3d (3d1, bilobular).
Titânio (Ti)
Z: 22 (22 e-1 22 p+1 22 n0)
Configuração eletrônica: [Ar] 4s2 3d2
DFC: 800 nm. Titânio. Segundo orbital 3d (3d2, bilobular).
Vanádio (V)
Z: 23 (23 e-1 23 p+1 23 n0)
Configuração eletrônica: [Ar] 4s2 3d3
DFC: 800 nm. Vanádio. Terceiro orbital 3d (3d3, lobular com tórus).
Crômio (Cr)
Z: 24 (24 e-1 24 p+1 24 n0)
Configuração eletrônica: [Ar] 4s2 3d4
DFC: 800 nm. Crômio. Quarto orbital 3d (3d4, bilobular).
Manganês (Mn)
Z: 25 (25 e-1 25 p+1 25 n0)
Configuração eletrônica: [Ar] 4s2 3d5
DFC: 800 nm. Manganês. Quinto orbital 3d (3d5, bilobular).
Ferro (Fe)
Z: 26 (26 e-1 26 p+1 26 n0)
Configuração eletrônica: [Ar] 4s2 3d6
DFC: 800 nm. Ferro. Sexto orbital 3d (3d6, bilobular).
Cobalto (Co)
Z: 27 (27 e-1 27 p+1 27 n0)
Configuração eletrônica: [Ar] 4s2 3d7
DFC: 800 nm. Crômio. Sétimo orbital 3d (3d7, bilobular).
Níquel (Ni)
Z: 28 (28 e-1 28 p+1 28 n0)
Configuração eletrônica: [Ar] 4s2 3d8
DFC: 800 nm. Níquel. Oitavo orbital 3d (3d8, lobular com tórus).
Cobre (Cu)
Z: 29 (29 e-1 29 p+1 29 n0)
Configuração eletrônica: [Ar] 4s2 3d9
DFC: 800 nm. Cobre. Nono orbital 3d (3d9, bilobular).
Zinco (Zn)
Z: 30 (30 e-1 30 p+1 30 n0)
Configuração eletrônica: [Ar] 4s2 3d10
DFC: 800 nm. Zinco. Décimo orbital 3d (3d10, bilobular).
Orbitais 4p
Gálio (Ga)
Z: 31 (31 e-1 31 p+1 31 n0)
Configuração eletrônica: [Ar] 4s2 3d10 4p1
DFC: 800 nm. Gálio. Primeiro orbital 4p (4p1, lobular).
Germânio (Ge)
Z: 32 (32 e-1 32 p+1 32 n0)
Configuração eletrônica: [Ar] 4s2 3d10 4p2
DFC: 800 nm. Germânio. Segundo orbital 4p (4p2, lobular).
Arsênio (As)
Z: 33 (33 e-1 33 p+1 33 n0)
Configuração eletrônica: [Ar] 4s2 3d10 4p3
DFC: 800 nm. Arsênio. Terceiro orbital 4p (4p3, lobular).
Selênio (Se)
Z: 34 (34 e-1 34 p+1 34 n0)
Configuração eletrônica: [Ar] 4s2 3d10 4p4
DFC: 800 nm. Selênio. Quarto orbital 4p (4p4, lobular).
Bromo (Br)
Z: 35 (35 e-1 35 p+1 35 n0)
Configuração eletrônica: [Ar] 4s2 3d10 4p5
DFC: 800 nm. Bromo. Quinto orbital 4p (4p5, lobular).
Kriptônio (Kr)
Z: 36 (36 e-1 36 p+1 36 n0)
Configuração eletrônica: [Ar] 4s2 3d10 4p6
DFC: 800 nm. Kriptônio. Sexto 4p (4p6, lobular).